Цель. Оценка непосредственных результатов энуклеации и резекционных вмешательств при нейроэндокринных опухолях поджелудочной железы G1–G2.
Материал и методы. В исследование включен 171 пациент с нейроэндокринными опухолями поджелудочной железы G1–G2. Панкреатодуоденальная резекция выполнена 25 больным, дистальная резекция – 60, энуклеация – 86.
Результаты. В цефалоцервикальном сегменте поджелудочной железы нейроэндокринные опухоли выявлены у 79 пациентов. Энуклеация опухоли выполнена в 54 наблюдениях, панкреатодуоденальная резекция – в 25. Осложнения после энуклеации развились у 22 (40,7%) пациентов, умер 1; после панкреатодуоденальной резекции осложнения выявлены у 9 (36%) больных, умер 1. В корпорокаудальном сегменте нейроэндокринные опухоли локализовались у 92 человек. Энуклеация выполнена в 32 наблюдениях, дистальная резекция поджелудочной железы – в 60. Осложнения после энуклеации отмечены у 5 (15,6%) пациентов, после дистальной резекции – у 27 (45,5%).
Заключение. При высокодифференцированных нейроэндокринных опухолях возможно выполнение энуклеации опухоли. Объем операции определяется размером опухоли, локализацией относительно протока поджелудочной железы, а также личным решением хирурга.
Идентификаторы и классификаторы
Нейроэндокринные опухоли (НЭО) поджелудочной железы (ПЖ) составляют менее 3% всех новообразований этого органа [1, 2]. Хирургическое вмешательство является основным методом лечения при НЭО ПЖ.
Список литературы
1. Perry R.R., Feliberti E.C., Hughes M.S. Management of pancreatic neuroendocrine tumors: surgical strategies and controversies. Endocr. Pract. 2024; 30 (10): 908-916. DOI: 10.1016/j.eprac.2024.07.010
2. Nagtegaal I.D., Odze R.D., Klimstra D., Paradis V., Rugge M., Schirmacher P., Washington K.M., Carneiro F., Cree I.A.; WHO Classification of Tumours Editorial Board. The 2019 WHO classification of tumours of the digestive system. Histopathology. 2020; 76 (2): 182-188. DOI: 10.1111/his.13975
3. Kohno S. Diagnosis and surgical treatment of gastro-enteropancreatic neuroendocrine neoplasms: a literature review. CancerDiagn. Progn. 2022; 2 (2): 115-125. DOI: 10.21873/cdp.10085
4. Bolm L., Nebbia M., Wei A.C., Zureikat A.H., Fernandez-Del Castillo C., Zheng J., Pulvirenti A., Javed A.A., Sekigami Y., Petruch N., Qadan M., Lillemoe K.D., He J., Ferrone C.R.; PAncreatic Neuroendocrine Disease Alliance (PANDA). Longterm outcomes of parenchyma-sparing and oncologic resections in patients with nonfunctional pancreatic neuroendocrine tumors №3 cm in a large multicenter cohort. Ann. Surg. 2022; 276 (3): 522-531. DOI: 10.1097/SLA.0000000000005559
5. Солодкий В.А., Кригер А.Г., Ахаладзе Г.Г., Гоев А.А., Гончаров С.В., Горин Д.С., Загайнов В.Е., Кузнецов Н.С., Кучин Д. М., Латкина Н.В., Лысанюк М. В., Майстренко Н.А., Мартиросян Т.А., Ромащенко П.Н., Шуинова Е.А., Юкина М.Ю. Энуклеация опухолей поджелудочной железы (многоцентровое исследование). Хирургия. Журнал им. Н.И. Пирогова. 2023; 2: 13-20.
Solodkiy V.A., Kriger A.G., Akhaladze G.G., Goey A.A., Goncharov S.V., Gorin D.S., Zagainov V.E., Kuznetsov N.S., Kuchin D.M., Latkina N.V., Lysanuk M.V., Maistrenko N.A., Martirosyan T.A., RomasAenko P.N., Shuinova E.A., Yukina M.Y. Enucleation of pancreatic tumors: a multiple-center study. Pirogov Russian Journal of Surgery. 2023; 2: 13-20. (In Russian). DOI: 10.17116/hirurgia202302113
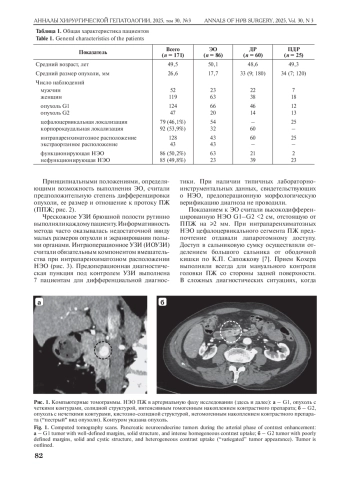
6. Белоусова Е.Л., Кармазановский Г.Г., Кубышкин В.А., Калинин Д.В., Кригер А.Г., Глотов А.В., Калдаров А.Р КТ-признаки, позволяющие определить оптимальную тактику лечения при нейроэндокринных опухолях поджелудочной железы. Медицинская визуализация. 2015; 5: 73-82.
Belousova E.L., Karmazanovsky G.G., Kubyshkin V.A., Kalinin D.V., Kriger A.G., Glotov A.V., Kaldarov A.R. CT features predict the optimal therapeutic approach for pancreatic neuroendocrine neoplasms. Medical Visualization. 2015; 5: 73-82. (In Russian).
7. Колченогов П.Д. К технике абдоминальной гастрэктомии по К.П. Сапожкову с применением муфты из мезоколона. Вестник хирургии имени И.И. Грекова. 1957; 78 (6): 23-27.
Kolchenogov P.D. K.P. Sapozhkov’s method of abdominal gastrectomy using mesocolon flap. Grekov’s Bulletin of Surgery. 1957; 78 (6): 23-27. (In Russian).
8. Солодкий В.А., Кригер А.Г., Горин Д.С., Загайнов В.Е., Кузнецов Н.С., Латкина Н.В., Майстренко Н.А., Мартиросян ТА., Шуинова Е.А. Панкреатодуоденальная резекция - результаты и перспективы (двухцентровое исследование). Хирургия. Журнал им. Н.И. Пирогова. 2023; 5: 13-21.
Solodkiy V.A., Kriger A.G., Gorin D.S., Zagainov V.E., Kuznetsov N.S., Latkina N.V., Maistrenko N.A., Martirosyan T.A., Shuinova E.A. Pancreaticoduodenectomy - results and prospects (two-center study). Pirogov Russian Journal of Surgery. 2023; 5: 13-21. (In Russian). DOI: 10.17116/hirurgia202305113
9. Claudio B., Giovanni M., Christos D., Micheal S., Mohammad A.H., Mustapha A., Peter A., Roland A., Horacio J.A., Marc G.B., Kevin C., Marco D.C., Massimo F., Laureano F., Carlos F.C., Abe F., Helmut F., Dirk J.G., Thilo H., Jakob I., Keith D.L., John PN., Attila O., Richard S., Shailesh V.S., Tadahiro T., Kyoichi T., William T., Charles V., Christopher L.W., Charles J.Y., Roberto S., Marcus B. Corrigendum to “The 2016 update of the International Study Group (ISGPF) definition and grading of postoperative pancreatic fistula: eleven years after”. Surgery. 2017; 161 (3): 584-591. Surgery. 2024; 176 (3): 988-989. DOI: 10.1016/j.surg.2024.05.043
10. Wente M.N., Veit J.A., Bassi C., Dervenis C., Sarr M.G., Abu Hilal M., Adham M., Allen P., Andersson R., Asbun H.J., Besselink M.G., Conlon K., Del Chiaro M., Falconi M., Fernandez-Cruz L., Fernandez-del Castillo C., Fingerhut A., Friess H., Gouma D.J., Hackert T., Izbicki J., Lillemoe K.D., Neoptolemos J.P., Olah A., Schulick R., Shrikhande S.V., Takada T., Takaori K., Traverso W.L., Vollmer C.M., Wolfgang C.L., Yeo C.J., Salvia R., Buchler M.W. Postpancreatectomy hemorrhage (PPH): an International Study Group of Pancreatic Surgery (ISGPS) definition. Surgery. 2007; 142 (1): 20-25. https://. DOI: 10.1016/j.surg.2007.02.001
11. Wente M.N., Bassi C., Dervenis C., Sarr M.G., Abu Hilal M., Adham M., Allen P., Andersson R., Asbun H.J., Besselink M.G., Conlon K., Del Chiaro M., Falconi M., Fernandez-Cruz L., Fingerhut A., Friess H., Gouma D.J., Hackert T., Izbicki J., Lillemoe K.D., Neoptolemos J.P., Olah A., Schulick R., Shrikhande S.V., Takada T., Takaori K., Traverso W.L., Vollmer C.M., Wolfgang C.L., Yeo C.J., Salvia R., Buchler M.W. Delayed gastric emptying (DGE) after pancreatic surgery: a suggested definition by the International Study Group of Pancreatic Surgery (ISGPS). Surgery. 2007; 142 (5): 761-768. DOI: 10.1016/j.surg.2007.05.005
12. Горбунова В.А. Нейроэндокринные опухоли. Общие принципы диагностики и лечения. М.: Кодекс, 2015. 455 с.
Gorbunova V.A. Nejroendokrinnye opuholi. Obshchie principy diagnostiki i lecheniya [Neuroendocrine tumors. General guidelines for diagnosis and management.] Moscow: Kodeks, 2015. 455 p. (In Russian).
13. Lloyd R.V., Osamura R.Y., Kloppel G., Rosai J., editors. WHO classification of tumours of endocrine organs. Lyon: World Health Organization; 2017. ISBN: 978-92-832-4493-6
14. Patrone R., Mongardini F.M., Conzo A., Principi M., Mazzella V. Pancreatic neuroendocrine tumors: what is the best surgical option? J. Clin. Med. 2024; 13 (10): 3015. DOI: 10.3390/jcm13103015
15. Acher A.W., Hallet J. Advances in management of nonfunctional pancreas neuroendocrine tumors. Surg. Clin. North Am. 2024; 104 (5): 1095-1111. DOI: 10.1016/j.suc.2024.03.010
16. Кондрашин С.А., Егоров А.В., Пашкова И.Л., Лотов А.Н., Силина Т.Л., Орлов С.Ю., Аскендерова Э.О. Эндоскопическое ультразвуковое исследование в дооперационной топической диагностике органического гиперинсулинизма. Ультразвуковая и функциональная диагностика. 2006; 2: 21.
Kondrashin S.A., Egorov A.V., Pashkova I.L., Lotov A.N., Silina T.L., Orlov S.Yu., Askenderova E.O. Endoscopic ultrasonography in the preoperative topical diagnosis of organic hyperinsulinism. Ultrasound and Functional Diagnostics. 2006; 2: 21. (In Russian).
17. Okabayashi T., Shima Y., Sumiyoshi T., Kozuki A., Ito S., Ogawa Y., Kobayashi M., Hanazaki K. Diagnosis and treatment of insulinoma. World J. Gastroenterol. 2013; 19 (6): 829-837. DOI: 10.3748/wjg.v19.i6.829
18. Lee L., Ito T., Jensen R.T. Imaging of pancreatic neuroendocrine tumors: recent advances, current status, and controversies. Expert. Rev. Anticancer Ther. 2018; 18 (9): 837-860. DOI: 10.1080/14737140.2018.1496822
19. Hiramoto J.S., Feldstein VA., Laberge D.M., Norton J.A.Intraoperative ultrasound and preoperative localization reveal all latent insulinomas; discussion 1025-1026. Arch. Surg. 2001; 136 (9): 1020-1025. DOI: 10.1001/archsurg.136.9.1020
20. Beane J.D., Borrebach J.D., Billderback A., Wells A., Miller F., Goodman Z. Small pancreatic neuroendocrine tumors: resect or enucleate? Am. J. Surg. 2021; 222 (1): 29-34.
Выпуск
Другие статьи выпуска
Руководящие принципы по лечению панкреатических кистозных новообразований (ПКН), основанные на доказательствах, отсутствуют. Это руководство является совместной инициативой Европейской исследовательской группы по кистозным опухолям поджелудочной железы (ПЖ), Объединения европейских гастроэнтерологов, Европейского клуба панкреатологов, Европейско-Африканской ассоциации гепатопанкреатобилиарной системы, Европейской хирургии пищеварительного тракта и Европейского общества гастроинтестинальной эндоскопии. Оно заменяет Европейские консенсусные рекомендации 2013 г. по ПКН.
Цель. Анализ современных методов диагностики и эндоскопического лечения при вирсунголитиазе, а также демонстрация клинического наблюдения успешного применения этапного эндоскопического лечения.
Материал и методы. Проведен анализ литературы и описано клиническое наблюдение пациентки с вирсунголитиазом, осложненным острой блокадой большого сосочка двенадцатиперстной кишки.
Результаты. Эндоскопические технологии позволили устранить обструкцию большого сосочка, удалить конкременты, восстановить проходимость протоков, избежать открытого оперативного вмешательства на поджелудочной железе. После трех этапов лечения (папиллотомия, литэкстракция, рестентирование) достигнута нормализация состояния больной и лабораторных показателей.
Заключение. Эндоскопические методы (литотрипсия, стентирование) – стандарт лечения при вирсунголитиазе благодаря минимальной инвазивности, эффективности и малому риску рецидива. Однако осложнения стентирования требуют строгого контроля. Клиническое наблюдение подтверждает необходимость поэтапного подхода и разработки стандартизованных протоколов для оптимизации результатов лечения.
Цель: определение факторов, влияющих на наличие остаточных камней после холедохоскопии и литотрипсии.
Материал и методы. В нашем ретроспективном исследовании принял участие 201 пациент с гепатолитиазом и стенозом желчных протоков. С января 2018 г. по декабрь 2020 г. все пациенты перенесли холедохоскопическую литотрипсию с рассечением или без рассечения паренхимы и резекцией печени в отделении гепатобилиарной хирургии в больнице VietDuc University (Ханой, Вьетнам). Были собраны демографические данные, выявлены клинические особенности, получены результаты лабораторных исследований, установлен тип операции и особенности стеноза желчных протоков (локализация, число, степень выраженности). Основным критерием оценки была частота полного удаления камней в послеоперационном периоде.
Результаты. У 82,6% пациентов был выявлен один участок стеноза, у 49,8% – несколько участков. Частота полного удаления камней после холедохоскопической литотрипсии составила 43,2%, а в сочетании с резекцией печени или рассечением паренхимы – 75,3%. Использование нескольких методов лечения и тип внутри печеночных камней являются двумя факторами, влияющими на наличие остаточных камней после операции.
Заключение. Холедохоскопия является эффективным способом диагностики желчных камней и выявления особенностей желчных протоков. Резекция печени и рассечение паренхимы в сочетании с холедохоскопической литотрипсией представляют собой безопасный и эффективный метод лечения, повышающий частоту полного удаления камней при гепатолитиазе и стенозе желчных протоков. В осложненных случаях, связанных с внутрипеченочными камнями, необходимо комплексное и интенсивное лечение.
Цель. Оценить роль выбора эндоскопической операции при лечении пациентов с аденомами большого сосочка двенадцатиперстной кишки, используя разработанную эндоскопическую классификацию аденом.
Материал и методы. С 2000 по 2024 г. выполнено эндоскопическое удаление аденом большого сосочка двенадцатиперстной кишки 200 пациентам. В 165 наблюдениях на этапе диагностики применяли эндо-УЗИ, в 35 наблюдениях метод не применяли.
Результаты. Технический успех при эндоскопическом удалении аденом большого сосочка двенадцатиперстной кишки в обеих группах составил 100%. Частота послеоперационных осложнений в основной группе составила 16,9%, в группе сравнения – 40%. В отдаленном периоде наблюдения частота рецидива аденомы составила 6,6% в основной группе и 20% – в группе сравнения.
Заключение. Персонифицированный выбор оптимального метода оперативного вмешательства для удаления аденом большого сосочка двенадцатиперстной кишки в зависимости от классификационного типирования новообразования позволяет минимизировать риск послеоперационных осложнений и улучшить радикальность вмешательства.
Цель. Изучить роль локализации и гистогенеза опухолей в качестве фактора риска осложнений и летального исхода после мультивисцеральных операций с панкреатодуоденальной резекцией.
Материал и методы. В исследование включили всех пациентов (n = 251), которые перенесли мультивисцеральную операцию с панкреатодуоденальной резекцией по поводу опухолей различных локализаций в двух лечебных учреждениях.
Результаты. При сравнительном анализе плотности поджелудочной железы достоверные различия получены между раком поджелудочной железы и раком большого сосочка двенадцатиперстной кишки (p = 0,012), раком дистального отдела общего желчного протока (p = 0,040), опухолями двенадцатиперстной кишки (p < 0,001), вторичными опухолями поджелудочной железы (p < 0,001), раком толстой кишки (p < 0,001), раком почки (p = 0,027), раком желудка (p < 0,001). Также достоверные различия получены при анализе пар рак большого сосочка двенадцатиперстной кишки – рак толстой кишки (p = 0,010); нейроэндокринная опухоль головки поджелудочной железы – рак толстой кишки (p < 0,001); нейроэндокринная опухоль поджелудочной железы – рак желудка (p = 0,006). При сравнительном анализе диаметра протока поджелудочной железы различия были достоверны между опухолями двенадцатиперстной кишки и раком поджелудочной железы (p = 0,016), раком толстой кишки и раком поджелудочной железы (p < 0,001), раком желудка и раком поджелудочной железы (p = 0,016). Частота послеоперационных осложнений во всей исследуемой группе составила 65,7% (n = 165), летальность – 7,2% (n = 18). Вероятность развития панкреатического свища достоверно увеличивалась при раке дистального отдела общего желчного протока (AOR 5,9; 95% ДИ 1,4–24,6; p = 0,015), при вторичных опухолях головки поджелудочной железы (AOR 4,7; 95% ДИ 1,06–21,0; p = 0,041), при раке желудка (AOR 2,8; 95% ДИ 1,048–7,691; p = 0,040). Вероятность развития несостоятельности панкреатодигестивного анастомоза больше при раке дистального отдела общего желчного протока (AOR 7,8; 95% ДИ 1,7–35,05; p = 0,007). При вторичных злокачественных новообразованиях головки поджелудочной железы вероятность летального исхода после операции достоверно больше (AOR 9,7; 95% ДИ 1,79–52,8; p = 0,008).
Заключение. Локализация и гистогенез опухоли могут быть независимыми факторами, определяющими непосредственный исход мультивисцеральной операции с панкреатодуоденальной резекцией. Протоковый рак головки поджелудочной железы является наиболее благоприятным гистотипом опухоли и локализацией в плане риска послеоперационных осложнений. Операции при раке общего желчного протока, метастатических опухолях головки поджелудочной железы, раке желудка сопровождаются значимо худшими непосредственными исходами.
Внутрипротоковые папиллярные муцинозные неоплазии представляют собой кистозные новообразования поджелудочной железы с риском малигнизации. Обзор затрагивает современные рекомендации по лечению пациентов с этим заболеванием, показания к хирургическому вмешательству, результаты оперативного лечения и стратегии наблюдения за пациентами. В нем также освещены последние достижения в мини-инвазивной хирургии и новые биомаркеры, направленные на совершенствование распределения рисков по уровням и сокращение числа неоправданных оперативных вмешательств.
Цель. Анализ последних взглядов на концепцию злокачественной прогрессии внутрипротоковой папиллярной муцинозной опухоли поджелудочной железы и наиболее значимых перспектив научных исследований в этой области.
Материал и методы. Обзор литературных данных, анализ данных канцер-регистра г. Москвы.
Результаты. Приведены наиболее значимые молекулярно-генетические исследования за последние десятилетия. На примере анализа данных операционного материала по кодам ICD-O г. Москвы за 2023–2024 гг. рассмотрены основные трудности морфологической диагностики внутрипротоковой папиллярной муцинозной опухоли поджелудочной железы с ассоциированной инвазивной карциномой.
Заключение. Геномные изменения во внутрипротоковой папиллярной муцинозной опухоли поджелудочной железы как фоновые поражения для протокового рака поджелудочной железы, обусловливающие их генетическую гетерогенность, имеют большое клиническое значение для понимания поликлональной теории развития рака, поиска новых мишеней и подходов в терапии. Ассоциированный инвазивный компонент во внутрипротоковой папиллярной муцинозной опухоли поджелудочной железы, согласно своему молекулярному профилю, чаще является генетически независимым.
Цель. Оптимизация комплексной дифференциальной диагностики кистозных новообразований поджелудочной железы внедрением в клиническую практику новых технологий эндоскопического УЗИ (эндо-УЗИ).
Материал и методы. Проведен анализ результатов комплексной диагностики 424 пациентов с кистозными новообразованиями поджелудочной железы, которым было выполнено эндо-УЗИ.
Результаты. В 328 (77,4%) наблюдениях при эндо-УЗИ было достаточно данных стандартного В-режима. В 96 (22,6%) наблюдениях была необходимость в контрастном усилении: 59 (61,5%) больным выполнили оценку накопления контрастного препарата стенкой, перегородками и солидными структурами, 25 (26%) – только стенкой и перегородками, 12 (12,5%) больным выполнили оценку нодулярного компонента кистозных новообразований поджелудочной железы. Ретроспективно установлено, что использование эндо-УЗИ с контрастным усилением по сравнению с В-режимом повысило общую точность метода в дифференциальной диагностике кистозных неоплазий и постнекротических кист на 14,7%, в диагностике солидных структур кистозных новообразований – на 11,3%, в диагностике кистозно-трансформированной аденокарциномы или ассоциированной с аденокарциномой внутрипротоковой папиллярной муцинозной неоплазии – на 9,9%. Внедрение в алгоритм комплексного эндо-УЗИ контрастного усиления способствовало уменьшению числа тонкоигольных пункций.
Заключение. Собственный опыт и мнение зарубежных исследователей свидетельствуют о необходимости включения в диагностический алгоритм кистозных новообразований поджелудочной железы мультимодального эндо-УЗИ. На основании результатов исследования разработан алгоритм применения новых технологий эндо-УЗИ в дифференциальной диагностике кистозных новообразований поджелудочной железы.
Цель. Анализ результатов лечения пациентов с кистозными опухолями поджелудочной железы в условиях экспертного центра гепатопанкреатобилиарной хирургии.
Материал и методы. С 2014 по 2025 г. выполнено 386 резекций поджелудочной железы, из них 82 (21,24%) по поводу кистозных опухолей. Средний возраст пациентов составил 51 ± 10,7 года, 63,4% больных – женщины.
Результаты. Десять (12,1%) пациентов оперировано по поводу муцинозной неоплазии боковых протоков поджелудочной железы, 13 (15,88%) – по поводу муцинозной неоплазии протока поджелудочной железы. Также оперировали 25 (30,53%) больных с муцинозно-кистозной неоплазией, 1 (1,21%) – с кистозной эндокринной опухолью, 21 (25,63%) – по поводу солидной псевдопапиллярной неоплазии, 12 (14,63%) больных с серозной цистаденомой. При ретроспективном патогистологическом анализе 121 наблюдения рака головки поджелудочной железы после панкреатодуоденальной резекции установлено, что у 31 (25,61%) пациента аденокарцинома развилась на фоне муцинозной неоплазии протока поджелудочной железы различных типов.
Заключение. Кистозные опухоли поджелудочной железы представляют собой новообразования с вариабельным биологическим поведением, что требует дифференцированного подхода к диагностике и лечению.
В 2023 г. по согласованию с руководством Ассоциации гепатопанкреатобилиарных хирургов стран СНГ было инициировано и проведено согласительное исследование по диагностике, лечению и наблюдению пациентов с серозными и муцинозными неоплазиями поджелудочной железы. На основании литературных справок были сформулированы ответы на каждый из 22 вопросов, оформленные в виде Консенсуса. В подготовке Консенсуса приняли участие 44 эксперта, представляющие 27 учреждений в 9 странах. Голосование проводили по методу Делфи, и в конечном итоге, включая результаты голосования по ряду положений на итоговой конференции, по всем вопросам был достигнут консенсус.
Уважаемые коллеги! По решению и при всесторонней поддержке редакции в очередном номере “Анналов хирургической гепатологии” нами подготовлен раздел, посвященный диагностике и лечению пациентов с кистозными новообразованиями поджелудочной железы. Актуальность тематики, на наш взгляд, очевидна. Улучшение доступности инструментальных методов диагностики, таких как КТ и МРТ, приводит к значительному росту выявляемости кистозных неоплазий поджелудочной железы. При этом ввиду значительной разнородности семиотики и сложностей определения прогноза при различных видах кистозных образований в профессиональном сообществе происходит множество дискуссий в части определения тактических подходов к лечению таких больных. Существующие рекомендации зачастую предлагают различную тактику, разные базовые критерии для ее выбора, что затрудняет их использование на практике. Особые сложности возникают, когда такие пациенты проходят лечение и наблюдаются в общесоматических не узкоспециализированных медицинских учреждениях.
Игорь Евгеньевич Хатьков – академик РАН, директор Московского клинического научного центра имени А. С. Логинова, главный внештатный специалист-онколог Департамента здравоохранения города Москвы.
Издательство
- Издательство
- ИЗДАТЕЛЬСКИЙ ДОМ ВИДАР-М
- Регион
- Россия, Москва
- Почтовый адрес
- Москва, 109028, а/я 16
- Юр. адрес
- 109004, г Москва, Таганский р-н, Тетеринский пер, д 16, помещ IV, ком 2
- ФИО
- Жариков Леонид Анатольевич (ГЕНЕРАЛЬНЫЙ ДИРЕКТОР)
- Контактный телефон
- +7 (___) _______
- Сайт
- http://www.vidar.ru/