Повышение содержания антиоксидантов в зерне пшеницы является актуальной общемировой тенденцией наряду с увеличением урожайности. С использованием ДНК-маркеров к генам биосинтеза антоцианов были выделены три гибридные линии с черной окраской зерна и шесть - с фиолетовой и светло-фиолетовой в потомстве от скрещивания образца к-44126 Triticum petropavlovskyi и линии сорта мягкой пшеницы Саратовская 29 - С29чз4. Все изученные линии, независимо от окраски зерна, имели более крупную зерновку относительно С29чз4, достигающую 53-59 мг у линий со светло-фиолетовым зерном. При этом Л1 и Л2 с черным зерном, а также Л7, Л8 и Л9 со светло-фиолетовым, несмотря на снижение числа колосков и зерен в колосе, демонстрировали увеличение массы зерен с колоса и растения в 1.3-2.1 раза по сравнению с С29чз4, а Л2 имела максимальное число зерен с растения, на 44 % превышающее показатель С29чз4. Наиболее высоким содержанием антоцианов характеризовались чернозерные Л1 и Л2, а Л7 со светло-фиолетовой окраской зерна не уступала линиям с фиолетовой окраской по содержанию антоцианов и фенольных соединений, а также по показателям антиоксидантной активности, но отличалась более высокой продуктивностью.
Идентификаторы и классификаторы
Зерно пшеницы может иметь голубовато-серую, фиолетовую и темно-коричневую (черную) окраску в зависимости от синтеза и накопления АЦ в различных слоях зерновки. Присутствие АЦ в перикарпе, основную долю которых составляет цианидин-3-глюкозид, придает зерну фиолетовую окраску. Производные дельфинидина (дельфинидин-3-глюкозид и дельфинидин-3-рутинозид) окрашивают алейроновый слой в голубой цвет (Hosseinian et al., 2008; Ficco et al., 2014; Iannucci et al., 2022). Черная окраска, в свою очередь, определяется одновременным накоплением АЦ, среди которых преобладают цианидин-3-глюкозид, цианидин-3,5- диглюкозид, дельфинидин-3-глюкозид, дельфинидин-3-галактозид и мальвидин-3-глюкозид (Sharma N. et al., 2020; Shamanin et al., 2024), и в перикарпе, и в алейроновом слое. Синтез АЦ в алейроновом слое находится под контролем доминантных аллелей генов Ba, интрогрессированных в геном пшеницы от нескольких близкородственных видов злаков, включая Thinopyrum ponticum (Podp.) Barkworth & D. R. Dewey (Ba1 в хромосоме 4E) (Garg et al., 2022). Фиолетовая окраска зерна контролируется комплементарным взаимодействием генов Pp-1 (Pp-A1, Pp-B1 и Pp-D1), локализованных в коротких плечах хромосом седьмой гомеологической группы (Khlestkina et al., 2010; Tereshchenko et al., 2012; Gordeeva et al., 2015), и Pp3 (TaMYC1), который интрогрессирован от Triticum aethiopicum Jakubz. в хромосому 2A (Shoeva et al., 2014).
Список литературы
1. Гордеева Е.И., Шоева О.Ю., Шаманин В.П., Хлесткина Е.К. Использование молекулярных маркеров в селекции мягкой пшеницы (Triticum aestivum L.) с различной антоциановой окраской зерновок. Письма в Вавиловский журнал генетики и селекции. 2023; 9(2):86-99. DOI: 10.18699/lettersvj-2023-9-11 EDN: SMDQQE
Gordeeva E.I., Shoeva O.Y., Shamanin V.P., Khlestkina E.K. The molecular markers applying in breeding of spring bread wheat (Triticum aestivum L.) lines with different anthocyanin coloration of the grains. Pisma v Vavilovskii Zhurnal Genetiki i Selektsii = Lett Vavilov J Genet Breed. 2023;9(2):86-99. (in Russian). DOI: 10.18699/LettersVJ-2023-9-11
2. Гультяева Е.И., Сибикеев С.Н., Дружин А.Е., Шайдаюк Е.Л. Расширение генетического разнообразия сортов яровой мягкой пшеницы по устойчивости к бурой ржавчине (Puccinia triticina Eriks.) в Нижнем Поволжье. Сельскохозяйственная биология. 2020;55(1):27-44. DOI: 10.15389/agrobiology.2020.1.27rus EDN: ENDKDT
Gultyaeva E.I., Sibikeev S.N., Druzhin A.E., Shaydayuk E.L. Enlargement of genetic diversity of spring bread wheat resistance to leaf rust (Puccinia triticina Eriks.) in Lower Volga region. Sel’skokhozyaistven naya Biologiya = Agricultural Biology. 2020;55(1):27-44. DOI: 10.15389/agrobiology.2020.1.27eng
3. Дружин А.Е., Сибикеев С.Н., Андреева Л.В. Использование вида Triticum petropavlovskyi Udacz. et Migusch. для расширения генетического разнообразия яровой мягкой пшеницы. Труды по прикладной ботанике, генетике и селекции. 2024;185(3):27-38. DOI: 10.30901/2227-8834-2024-3-27-37 EDN: CIAZRV
Druzhin A.E., Sibikeev S.N., Andreeva L.V. The use of the species Triticum petropavlovskyi Udacz. et Migusch. to expand the genetic diversity of spring bread wheat. Proceedings on Applied Botany, Genetics and Breeding. 2024;185(3):27-38. (in Russian). DOI: 10.30901/2227-8834-2024-327-37
4. Романов Б.В., Пимонов К.И., Липский Д.Д. Продукционные особенности пшеницы Triticum petropavlovskyi. Известия Нижневолжского агроуниверситетского комплекса: наука и высшее профессиональное образование. 2020;4(60):173-183. DOI: 10.32786/2071-9485-2020-04-16 EDN: VHEIDN
Romanov B.V., Pimonov K.I., Lipsky D.D. Productive features of wheat Triticum petropavlovskyi. Proceedings of Lower Volga Agro-University Complex: Science and Higher Education. 2020;4(60):173-183. (in Russian). DOI: 10.32786/2071-9485-2020-04-16
5. Савин Т.В., Абугалиева А.И., Чакмак И., Кожахметов К. Минеральный состав зерна диких сородичей и интрогрессивных форм в селекции пшеницы. Вавиловский журнал генетики и селекции. 2018;22(1):88-96. DOI: 10.18699/VJ18.335 EDN: YPNTVX
Savin T.V., Abugaliyeva A.I., Cakmak I., Kozhakhmetov K. Mineral composition of wild relatives and introgressive forms in wheat selection. Vavilovskii Zhurnal Genetiki i Selektsii = Vavilov J Genet Breed. 2018;22(1):88-96. (in Russian). DOI: 10.18699/VJ18.335
6. Удачин Р.А., Мигушова Э.Ф. Новое в познании рода Triticum L. Вестник сельскохозяйственной науки. 1970;9:20-24.
Udachin R.A., Migushova E.F. New in the knowledge of the genus Triticum L. Vestnik Sel’skokhozyaystvennoy Nauki = Herald of Agricultural Sciences. 1970;9:20-24 (in Russian).
7. Шоева О.Ю., Гордеева Е.И., Хлесткина Е.К. Внутригенный ДНК-маркер для отбора пшеницы с повышенным содержанием антоцианов в перикарпе зерновки. Патент № 2774444. 29.11.2021.
Shoeva O.Yu., Gordeeva E.I., Khlestkina E.K.Intragenic DNA marker for the selection of wheat with a high content of anthocyanins in the grain pericarp. Patent No. 2774444. 29.11.2021 (in Russian).
8. Abdel-Aal E.S.M., Hucl P. A rapid method for quantifying total anthocyanins in blue aleurone and purple pericarp wheats. Cereal Chem. 1999;76(3):350-354. DOI: 10.1094/CCHEM.1999.76.3.350
9. Bieńkowska T., Suchowilska E., Kandler W., Krska R., Wiwart M. Triticum polonicum L. as potential source material for the biofortification of wheat with essential micronutrients. Plant Genet Resour. 2019;17(3):213-220. DOI: 10.1017/S1479262118000394
10. Efremova T.T., Morozov S.V., Chernyak E.I., Chumanova E.V.Combining the genes of blue aleurone and purple pericarp in the genotype of spring bread wheat Saratovskaya 29 to increase anthocyanins in grain. J Cereal Sci. 2023;109:103616. DOI: 10.1016/j.jcs.2022.103616 EDN: CUQXMI
11. Fan Y., Wang Z., Hu S., Li Q., Liu F., Liu G., Ma M., Liu C. Uptake and preferential partitioning of zinc in different wheat species. Crop Sci. 2023;63(4):2426-2437. DOI: 10.1002/csc2.20988 EDN: BJHQJX
12. Ficco D.B.M., De Simone V., Colecchia S.A., Pecorella I., Platani C., Nigro F., Finocchiaro F., Papa R., De Vita P. Genetic variability in anthocyanin composition and nutritional properties of blue, purple, and red bread (Triticum aestivum L.) and durum (Triticum turgidum L. ssp. turgidum convar. durum) wheats. J Agric Food Chem. 2014;62(34):8686-8695. DOI: 10.1021/jf5003683
13. Garg M., Chawla M., Chunduri V., Kumar R., Sharma S., Sharma N.K., Kaur N., Kumar A., Mundey J.K., Saini M.K., Singh S.P. Transfer of grain colors to elite wheat cultivars and their characterization. J Cereal Sci. 2016;71:138-144. DOI: 10.1016/j.jcs.2016.08.004 EDN: XUCNUB
14. Garg M., Kaur S., Sharma A., Kumari A., Tiwari V., Sharma S., Kapoor P., Sheoran B., Goyal A., Krishania M. Rising demand for healthy foodsanthocyanin biofortified colored wheat is a new research trend. Front Nutr. 2022;9:878221. DOI: 10.3389/fnut.2022.878221
15. Gordeeva E.I., Shoeva O.Y., Khlestkina E.K. Marker-assisted development of bread wheat near-isogenic lines carrying various combinations of purple pericarp (Pp) alleles. Euphytica. 2015;203(2):469-476. DOI: 10.1007/S10681-014-1317-8 EDN: VACIAD
16. Gordeeva E., Shoeva O., Mursalimov S., Adonina I., Khlestkina E. Fine points of marker-assisted pyramiding of anthocyanin biosynthesis regulatory genes for the creation of black-grained bread wheat (Triticum aestivum L.) lines. Agronomy. 2022;12:2934. DOI: 10.3390/agronomy12122934 EDN: OVAWJG
17. Hosseinian F.S., Li W., Beta T. Measurement of anthocyanins and other phytochemicals in purple wheat. Food Chem. 2008;109(4):916-924. DOI: 10.1016/j.foodchem.2007.12.083
18. Iannucci A., Suriano S., Cancellaro S., Trono D. Anthocyanin profile and main antioxidants in pigmented wheat grains and related millstream fractions. Cereal Chem. 2022;99(6):1282-1295. DOI: 10.1002/cche.10591
19. Khlestkina E.K., Röder M.S., Börner A. Mapping genes controlling anthocyanin pigmentation on the glume and pericarp in tetraploid wheat (Triticum durum L.). Euphytica. 2010;171(1):65-69. DOI: 10.1007/s10681-009-9994-4 EDN: MWVNAV
20. Korzun V., Röder M., Worland A.J., Börner A.Intrachromosomal mapping of genes for dwarfing (Rht12) and vernalization response (Vrn1) in wheat by using RFLP and microsatellite markers. Plant Breed. 1997;116(3):227-232. DOI: 10.1111/j.1439-0523.1997.tb00987.x
21. Kukoeva T.V., Molobekova C.A., Totsky I.V., Vasiliev G.V., Pronozin A.Yu., Afonnikov D.A., Khlestkina E.K., Shoeva O.Yu. Enrichment of grain anthocyanin content through marker-assisted breeding for Ant1, Ant2 or HvMyc2 genes in barley (Hordeum vulgare L.). Agronomy. 2024;14(6):1231. DOI: 10.3390/agronomy14061231 EDN: HCWGOF
22. Kumari A., Sharma S., Sharma N., Chunduri V., Kapoor P., Kaur S., Goyal A., Garg M. Influence of biofortified colored wheats (purple, blue, black) on physicochemical, antioxidant and sensory characteristics of chapatti (Indian flatbread). Molecules. 2020;25(21):5071. DOI: 10.3390/molecules25215071 EDN: HGPMKD
23. Li X., Qian X., Lǚ X., Wang X., Ji N., Zhang M., Ren M. Upregulated structural and regulatory genes involved in anthocyanin biosynthesis for coloration of purple grains during the middle and late grainfilling stages. Plant Physiol Biochem. 2018;130:235-247. DOI: 10.1016/j.plaphy.2018.07.011
Выпуск
Другие статьи выпуска
В настоящее время особый интерес представляет установление влияния удвоения числа хромосом на селекци-онно значимые признаки в процессе селекции. В 2018-2021 гг. проведены полевые и лабораторные исследования с целью сравнительной оценки по хозяйственно ценным признакам и свойствам исходных диплоидных сортов ржи и полученных на их основе тетраплоидных аналогов в условиях Западной Сибири. Материалом для исследования послужили две пары аналогов: диплоидные сорта Короткостебельная 69 и Чулпан и их тетраплоидные формы Тетра короткая и Влада. Cравнительный анализ показал сходство признаков по высоте и зимостойкости растений при переходе с диплоидного на тетраплоидный уровень, так как наследование этих признаков носит полигенный характер, что благоприятно влияет на устойчивость растений к стрессу. У тетраплоидных аналогов отмечено достоверное увеличение урожайности на 17.2-23.5 % и крупности зерна в 1.2-1.5 раза. Следовательно, удвоение числа хромосом приводит к выраженности изменчивости признака урожайности и массы 1000 зе-рен. Кроме того, наблюдалось повышение массы зерна с колоса на 0.07-0.72 г и массы зерна с растения на 1.08-1.83 г, что в конечном итоге повысило урожайность по сравнению с исходными диплоидными формами. Установлено нежелательное влия-ние удвоения числа хромосом на такие признаки, как озерненность, продуктивная кустистость, натура зерна, число падения и вегетационный период. Таким образом, результаты исследования свидетельствуют о том, что полиплоидизация у ржи по-вышает эффективность использования в сельскохозяйственном производстве тетраплоидных сортов озимой ржи в условиях Западной Сибири благодаря высоким показателям зимостойкости, устойчивости к полеганию, урожайности и крупности зерна.
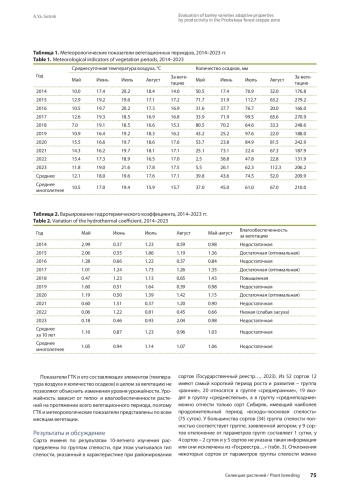
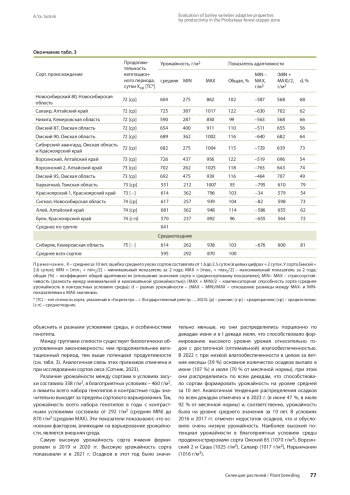
Цель работы - оценка адаптивного потенциала сортов ячменя, созданных в селекционных учреждениях Сибири, по урожайности в северной лесостепи Новосибирского Приобья. Исследования проводились в 2014-2023 гг. в севообороте Сибирского научно-исследовательского института растениеводства и селекции - филиала ФИЦ ИЦиГ СО РАН. Материалом исследования были 52 сорта ячменя, включенные в Госреестр РФ (районированные) по Западно-Сибирскому (10) и Восточно-Сибир скому (11) регионам. Сорта оценены по показателям: общая адаптивность к условиям внешней среды, устойчивость к экстремаль ным факторам по годам, стабильность формирования урожайности в контрастных условиях. Адаптивность сортов определяли по методике Л. А. Животкова с коллегами, устойчивость сортов к стрессовым условиям - по формулам в изложении А. А. Гончаренко, размах урожайности - по методике В. А. Зыкина с коллегами. Высокую общую адаптивность к условиям внешней среды показали сорта по группам спелости: раннеспелые - Червонец, Танай и Симон (100-102 %); среднеранние - Саша, Абалак, Колчан, Талан, Золотник, Омский 88, Омский 86 (107-117 %); среднеспелые - Салаир, Ворсинский, Ворсинский 2, Омский 85 (117-122 %). Наиболее высокий потенциал урожайности за 10 лет показали сорта: Омский 85 (1070 г/м2), Ворсинский 2, Саша (1025 г/м2), Салаир (1017 г/м2) и Нарымчанин (1016 г/м2). Устойчивость к стрессу (наименьшая разница между максимальной и минимальной урожайностями) имели сорта: раннеспелые - Заларинец, Червонец, Айхал, Алтан-Булаг (-371…-437 г/м2); среднеранние - Омский 88, Золотник, Паллидум 394 и Омский 80 (-237…-387 г/м2); среднеспелые - Красноярский 1, Омский 87, Ворсинский, Енисей, Обской и Никита (-434…-563 г/м2). Компенсаторной способностью (наибольшей средней урожайностью в контрастных условиях) характеризуются: раннеспелые - Танай, Червонец, Симон и Казьминский (550-591 г/м2); среднеранние - Колчан, Саша, Омский 90, Ворсинский, Абалак, Талан и Омский 86 (650-720 г/м2); среднеспелые - Омский 95, Салаир, Омский 85, Ворсинский и Омский 90 (682-707 г/м2). Стабильную урожайность в контрастных условиях продемонстрировали: раннеспелые - Червонец, Танай, Заларинец; среднеранние - Паллидум 394, Абалак, Колчан, Омский 80, Талан; среднеспелые - Омский 95, Красноярский 1, Ворсинский и Омский 87. Данные сорта рекомендуются для широкого использования в селекционном процессе.
Человек подвергается воздействию различных химических соединений на протяжении жизни, однако профессиональная специализация обуславливает наиболее опасное воздействие на организм. Важной проблемой является понимание влияния промышленной среды на геномную стабильность у работников. Известно, что контакт с угольной пылью и продуктами сжигания угля (особенно интенсивный в производственных условиях) способен негативно воздействовать на генетический аппарат человека. Тем не менее многие аспекты такого воздействия остаются малоизученными. В частности, пока мало известны эпигенетические эффекты действия производственных факторов и их взаимосвязь с накоплением геномных нарушений. Были обследованы 455 работников угольных теплоэлектростанций г. Кемерово и 448 жителей той же местности, не занятых на производстве. Генетические нарушения оценивались с помощью микроядерного теста с блоком цитокинеза в лимфоцитах крови. В анализ были включены такие показатели, как микроядра, нуклеоплазменные мосты и протрузии. Оценку статуса метилирования промоторных зон генов TP53, BRCA1 и ERCC2 проводили при помощи метил-специфической полимеразной цепной реакции. В результате исследования обнаружено повышение частоты встречаемости цитогенетических повреждений в клетках крови у работников угольных теплоэлектростанций, в отличие от группы сравнения. При изучении распределения степени метилирования промоторных областей генов TP53, BRCA1 и ERCC2 установлена наибольшая частота случаев гиперметилирования промоторов всех изученных генов у работников, в отличие от группы сравнения, что говорит о влиянии производственной среды угольных теплоэлектростанций. Выявлено увеличение частоты встречаемости микроядер, мостов и протрузий у рабочих с гиперметилированными промоторами генов TP53, BRCA1 и ERCC2. Наиболее выраженное изменение профиля метилирования наблюдалось у рабочих, возраст которых был более 50 лет, с производственным стажем выше 25 лет. Полученные данные свидетельствуют о наличии генетических и эпигенетических эффектов действия факторов производственной среды угольных теплоэлектростанций на геномную стабильность работников.
Мягкая пшеница Triticum aestivum L. является аллополиплоидом (2n = 6x = 42). Ее геном включает в себя геномы трех предковых видов, что позволяет хорошо переносить анеуплоидию ввиду наличия нескольких копий одних и тех же генов, находящихся в гомеологичных хромосомах. Это свойство было продемонстрировано на созданных на основе ряда сортов мягкой пшеницы анеуплоидных линиях. Отсутствие хромосомы 3В у мягкой пшеницы ведет к аномалиям мейотического деления, в том числе к снижению числа хиазм и асинапсису. Замещение хромосомы 3В мягкой пшеницы гомеологичной хромосомой 3R ржи Secale cereale L. приводит к нарушению хиазмообразования и асинапсису, нарушению компактизации хромосом, асинхронному поведению хромосом во втором делении мейоза и нарушениям в динамике микротрубочкового цитоскелета. Вероятно, в хромосоме 3R ржи, в отличие от гомеологичной хромосомы 3B мягкой пшеницы, отсутствуют гены, играющие ключевую роль в контроле нормального протекания мейоза у мягкой пшеницы. Цель данной работы - сравнительный анализ мейотических генов в хромосомах 3B и 3R мягкой пшеницы и диплоидной ржи соответственно. В результате проведенного анализа баз данных обнаружено, что в хромосоме 3R отсутствуют три мейотических гена: TraesCS3B02G308600 (ASK1/ASK2), TraesCS3B02G048300 (FANCM), TraesCS3B02G458900 (EMS1). При этом лишь для гена TraesCS3B02G308600 (ASK1/ASK2) показано отсутствие гомеологов в геноме мягкой пшеницы. На основе известных мейотических генов (mei-гены) мягкой пшеницы были построены и проанализированы генные сети. Гены TraesCS3B02G048300 (FANCM), TraesCS3B02G458900 (EMS1) располагались вне построенных генных сетей, тогда как ген TraesCS3B02G308600 (ASK1/ASK2) вместе с основными описанными генами мейоза формировал сеть из 22 генов. На основании полученных результатов сделано предположение, что отсутствие гена TraesCS3B02G308600 (ASK1/ASK2) у пшенично-ржаной замещенной линии 3R(3B) по большей части определяет характер аномалий мейотического процесса у пшенично-ржаной замещенной линии 3R(3B) Саратовская 29/рожь Онохойская.
Статистика статьи
Статистика просмотров за 2025 год.
Издательство
- Издательство
- НИИТПМ
- Регион
- Россия, Новосибирск
- Почтовый адрес
- 630089, г. Новосибирск, ул. Б. Богаткова, 175/1, Метро "Золотая нива", Автобус "Молодежная, Кошурникова"
- Юр. адрес
- 630090, г. Новосибирск, пр-т Академика Лаврентьева, 10
- ФИО
- Рагино Юлия Игоревна (Руководитель)
- Контактный телефон
- +7 (383) 3730981
- Сайт
- https://iimed.ru/