- Главная
- Реестр патентов
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ДИАГНОСТИКИ СИФИЛИСА С ИСПОЛЬЗОВАНИЕМ МЕТОДА ПРЯМОГО ПРОТЕОМНОГО ПРОФИЛИРОВАНИЯ СЫВОРОТКИ КРОВИ (57) Реферат: Изобретение относится к области медицины, в частности к способу диагностики сифилиса у пациента методом прямого протеомного профилирования сыворотки крови на основе выявления в опытном образце сыворотки биомаркеров сифилиса. Способ диагностики сифилиса предусматривает стадию фракционирования белков сыворотки с использованием магнитных частиц, масс-спектрометрический анализ образца элюата и анализ полученного масс-спектра на предмет наличия или отсутствия набора пиков, соответствующих биомаркерам сифилиса. Причем наличие характерного набора пиков в масс-спектре свидетельствует о наличии сифилиса, а отсутствие характерного набора пиков в масс-спектре свидетельствует об отсутствии сифилиса у пациента. 2 з.п. ф-лы, 4 табл. Область техники настоящего изобретения Настоящее изобретение относится к области медицины, конкретнее к диагностике инфекций, передаваемых половым путем, а именно сифилиса. Предшествующий уровень техники настоящего изобретения Сифилитическая инфекция относится к социально-значимым заболеваниям, т.е. заболеваниям, вызывающим выраженный общественный резонанс. Помимо экономического ущерба для общества, связанного с нарушением трудоспособности больного, определенными моральными и социальными конфликтами, данные заболевания таят в себе так называемую отсроченную опасность, которая может проявиться через многие годы в виде нарушения репродуктивного здоровья, рождения физически и умственно неполноценного потомства, тяжелых поражений нервной системы и различных внутренних органов. Итогом может стать снижение численности населения (увеличение смертности, уменьшение рождаемости), возрастание числа психически и умственно неполноценных граждан, инвалидов и т.п., что представляет реальную угрозу экономическому и общественному потенциалу страны [44]. Для предотвращения отдаленных последствий заболеваний ведущая роль принадлежит их раннему выявлению. В настоящее время для диагностики сифилитической инфекции применяют прямые методы, основанные на непосредственном выявлении возбудителя из очагов поражения, и непрямые, серологические методы для выявления антител к возбудителю заболевания. Наиболее убедительным доказательством инфицирования сифилисом является прямое обнаружение возбудителя инфекции, бледной трепонемы Treponema pallidum. В настоящее время наиболее широко применяется микроскопическое исследование материала в темном поле. Результат темнопольной микроскопии не всегда даст однозначный ответ о наличии инфекции. Отсутствие трепонем в типичных очагах поражения может быть обусловлено как снижением их количества в очаге в связи с длительностью его существования и предварительным лечением пациента (использование антибактериальных и антисептических препаратов), так и некачественной техникой взятия образца или исследования материала [13, 17]. Отрицательный результат не является основанием для исключения диагноза сифилиса и требует дальнейшего подтверждения серологическими методами диагностики. В то же время возможны ложноположительные результаты в связи с трудностью дифференцировки бледной трепонемы от других сапрофитных трепонем [22]. Для решения вышеуказанных проблем создаются новые методы диагностики, и наибольшее развитие получила полимеразная цепная реакция (ПЦР), которая в настоящее время носит исследовательский статус [15, 22, 35, 123, 160]. Тем не менее, прямое определение патогенных Treponema pallidum позволяет достоверно установить диагноз только при манифестных формах заболевания, т.е. когда имеются клинические проявления инфекции [17, 20, 113, 160]. По данным официальной статистической отчетности в последнее время преобладают скрытые формы сифилитической инфекции [45], диагностика которых основана на выявлении антител к Treponema pallidum. Таким образом, в настоящее время основными диагностическими методами являются серологические тесты, которые подразделяют на две группы: нетрепонемные, или неспецифические (НТТ), и трепонемные, или специфические (ТТ). В НТТ применяется антиген нетрепонемного происхождения (как правило, кардиолипин - лецитин - холестериновый антиген), в испытуемой сыворотке выявляются иммуноглобулины М и G (IgM и IgG) антитела к липидам клетоточной стенки Treponema pallidum. Исторически первым нетрепонемным серологическим тестом на сифилис стала адаптированная А.Вассерманом с соавт.(1906 г.) реакция связывания комплемента (РСК), в которой в качестве антигена был использован экстракт печени новорожденных с врожденным сифилисом. После работ Pangborn (1941 г.) [149], выделившего и очистившего кардиолипин, что в последующем позволило стандартизировать кардиолипин - лецитин - холестериновый антигенный комплекс, в РСК стали применять коммерческие препараты кардиолипинового антигена. Кроме РСК с кардиолипиновым антигеном (РСКк) к НТТ относят реакцию микропреципитации (РМП) и тест быстрых плазменных реагинов (RPR). НТТ используются в качестве отборочных тестов для скрининга большого количества людей и оценки эффективности терапии. В ряде случаев все тесты данной группы могут давать ложноотрицательные результаты (когда при наличии заболевания определяется отрицательный результат реакции), обусловленные феноменом прозоны, когда блокируется реакция антиген-антитело при избыточном количестве антител в исследуемой сыворотке, что наиболее часто наблюдается во вторичном периоде сифилитической инфекции (1-2%) [17, 114,], а также при обследовании пациентов с выраженной иммунной недостаточностью, ВИЧ-инфицированных [37, 80]. Кроме того, в НТТ регистрируется значительное количество (до 2,5%) ложноположительных результатов (ЛПР) (когда при отсутствии заболевания определяется положительный результат реакции) [29]. ЛПР могут быть обусловлены как экзогенными, зависящими от каких-то внешних моментов по отношению к организму человека, так и эндогенными, обусловленными происходящими в нем процессами, причинами. К числу экзогенных причин могут быть отнесены технические ошибки и погрешности при проведении исследования: нарушение условий и методики проведения реакции [30, 49], нестабильные характеристики антигена, выделенного из клеточных компонентов трепонем [36], различие ингредиентов, качества и рабочей дозы комплемента, сроки хранения сыворотки [31]. К эндогенным причинам, вызывающим ЛПР, относят генетические особенности отдельных индивидуумов, сопровождающиеся способностью к неспецифическим реакциям [27, 70, 83, 178], физико-химические изменения сыворотки крови [39], аутоиммунные нарушения [26, 49, 54, 72, 119], а также сдвиги в состоянии белкового и липидного обмена [29, 30, 46, 48, 51, 170]. Накопление липидов, участвующих в реагинных тестах, может происходить в тканях в результате разрушения клеточных митохондрий и высвобождения кардиолипина, входящего в состав митохондриальных мембран, что создает основу для развития неспецифической позитивности липидных тестов [29]. Ложноположительные результаты НТТ описаны при лепре [31], туберкулезе [159], малярии [98, 161], респираторных заболеваниях [191], диффузных болезнях соединительной ткани [71, 101, 110], дерматозах [95, 111], сахарном диабете [17], заболеваниях желудочно-кишечного тракта и печени [10, 28, 39], злокачественных новообразованиях [29], сердечно-сосудистой и гематологической патологии [54]. Среди заболеваний, вызываемых вирусами, ЛПР зарегистрированы при гриппе [1], ветряной оспе [79], гепатите [169, 173], ВИЧ-инфекции [33, 61, 85]. ЛПР могут сопровождать наркоманию и хронический алкоголизм [23, 67, 77, 99, 115, 154], отравления и интоксикации [29], отмечаться при таких физиологических состояниях, как беременность, менструация и преклонный возраст [4, 29, 54, 70], при вакцинации, многократной гемотрансфузии [4, 54]. ЛПР нередко наблюдаются у так называемых практически здоровых людей и могут являться преклиническими проявлениями тяжелых заболеваний [150], таких как системная красная волчанка, ревматизм, онкопатологии, воспалительные гинекологические заболевания, глубокий венозный тромбоз конечностей и некротическая пурпура [55, 112, 175]. Титры серологических реакций у лиц с ложноположительными результатами могут быть как низкими, колеблющимися [34, 147, 157], так и высокими [4, 49], что, несомненно, осложняет трактовку результатов реакции и затрудняет диагностику сифилитической инфекции. Попытки дифференциации истинноположительных результатов серологических реакций на сифилис от ЛПР издавна были связаны с усовершенствованием известных серологических методов диагностики [12, 32,49, 156, 177] и созданием принципиально новых. Результаты совершенствования тестов не получили широкого признания и не решили имеющуюся проблему. Переворот в дифференциации истинных и ложноположительных результатов серореакций на сифилис произошел в результате разработки трепонемных тестов (ТТ), в которых применяется антиген трепонемного происхождения. Они используются для подтверждения диагноза, распознавания ложноположительных результатов НТТ. Первым ТТ, предложенным в 1949 г. R.Nelson и M.Meyer [144], была РИБТ, или РИТ. Суть этой реакции заключается в потере подвижности бледной трепонемы в присутствии иммобилизирующих противотрепонемных антител сыворотки крови больных сифилисом и комплемента в условиях анаэробиоза. С течением времени стало известно, что РИТ, как и всякая другая биологическая реакция, не обладает абсолютной специфичностью [2, 3, 7, 29, 31, 40, 43, 58, 116, 140]. Так, Резайкина А.В. (1979) получила 0,4% ЛПР в РИТ при исследовании 2157 сывороток соматических больных [43], Пшеничная Л.А. (1971) выявила аналогичные результаты при злокачественных новообразованиях (0,27%), системной красной волчанке (3%), сердечно-сосудистой патологии (0,19%), пневмонии (0,66%), у беременных (0,34%) [40]. Неспецифическое выпадение положительных результатов РИТ отмечено у больных туберкулезом, генерализованным атеросклерозом, гипертиреозом, системной красной волчанкой, ревмокардитом, язвенной болезнью желудка и у практически здоровых лиц [58], у пациентов с миеломой, саркоидозом, сахарным диабетом, циррозом печени и болезнью Боткина [116, 140]. Значительный процент положительных (2,8%) и слабоположительных (2,2%) результатов РИТ отмечен у больных лепрой [116]. По мнению некоторых авторов РИТ совершенно непригодна для дифференциации сифилиса от трепонематозов (беджель, пинта и др.), при которых выявляется почти такой же процент положительных результатов, как и при сифилисе [29, 31]. Вместе с тем РИТ в ряде случаев не выявляет противосифилитических AT у больных с заведомым сифилисом, в особенности в ранних стадиях заболевания из-за малого количества иммобилизинов [2, 93, 187]. В 1953 году была разработана модификация РСК-РСК с трепонемным антигеном, приготовленным из непатогенных культуральных Treponema phagedenis (штамм Рейтер) [81], имеющих общие перекрестно-реагирующие антигены с Treponema pallidum. Этот тест давал значительное количество ложноположительных результатов при обследовании лиц с системными заболеваниями соединительной ткани, органов кроветворения, диабете, онкологических и воспалительных заболеваниях [29]. До 2006 года на территории Российской Федерации тест применялся в качестве отборочного в составе комплекса серологических реакций (КСР) наряду с РСК с кардиолипиновым антигеном и РМП. В настоящее время, в связи с разработкой более чувствительных, специфичных и менее трудоемких реакций, использование РСК с кардиолипиновым и трепонемным антигенами ограничивается и заменяется на современные ИФА и РПГА в сочетании с РМП (RPR) [38]. Следующей реакцией, которую до настоящего времени широко используют для диагностики сифилиса, стала РИФ, сочетающая в себе свойства иммунологического исследования, обеспечивающего специфичность, и люминесцентной микроскопии, обусловливающей высокую чувствительность теста [31]. Впервые примененная L.Borel и P.Durel в 1959 году в сифилидологической практике, обладая высокой чувствительностью и специфичностью при всех формах заболевания, РИФ является "золотым стандартом" диагностики сифилитической инфекции [17, 68]. Вместе с тем она не является абсолютно специфичной. По данным Larsen S.A. (1995) в специфических флюоресцентных тестах сыворотки приблизительно 1% людей дают ЛПР на сифилис [124]. Неспецифические результаты РИФ отмечены при системной красной волчанке, ревматоидном артрите, склеродермии, сахарном диабете, циррозе печени, генитальном герпесе, лепре, трепонематозах, беременности, после вакцинации, в старческом возрасте, при гипергаммаглобулинемии и др. [29, 31, 52, 53, 66, 124, 132]. РИБТ и РИФ являются сложными и трудоемкими тестами, требуют наличия вивария, так как для их постановки используют живые патогенные бледные трепонемы штамма Nihols, полученные из 7-10-дневного кроличьего орхита. Для современных трепонемных тестов ИФА и РПГА используют промышленные тест-системы. Они получили широкое распространение как скрининговые, так и подтверждающие тесты на сифилис [16, 18, 199], и, в соответствии с Приказом МЗ РФ Принцип ИФА заключается в соединении комплекса «антиген-антитело» с конъюгатом, содержащим ферментную метку, выявляемую с помощью субстратной смеси [18, 24, 31, 81, 182]. Существуют тест-системы для выявления IgM-антител, IgG-антител и IgM+IgG-антител, антител к различным компонентам Treponema pallidum -иммуноблотинг. Благодаря высокой чувствительности и специфичности, близкой РИФ, метод получил всеобщее признание [6, 16, 18, 20, 22, 42, 54, 63, 143]. Вместе с тем он, так же как и ранее описанные трепонемные реакции, не оказался абсолютно специфичным. Ложноположительные результаты описаны в 1,5-3,2% случаев [9, 125, 134, 158]. По мнению В.Ф.Ляхова (1991) в ИФА ЛПР могут быть получены за счет ревматоидного фактора, представляющего собой IgM против собственных IgG человека, а также перекрестно-реагирующих с трепонемным антигеном антител, образующихся при различных системных или индуцированных лекарствами, либо наркотиками нарушениях обмена [26]. На ревматоидный фактор, как на причину ЛПР у новорожденных детей указывает Mezzardra G. (1983) [138]. Кроме того, у плода или ребенка IgM-антитела могут образовываться к IgG-антителам матери, попавшим в его организм трансплацентарным путем [8, 18, 26, 41, 47, 124, 138, 155]. Необходимым условием достоверности исследования служит безупречная точность в разделении сывороток на классы иммуноглобулинов (IgM, IgG), так как присутствие в сыворотке даже небольших количеств IgG может дать ложноположительную реакцию по механизму конкурентного торможения [103, 130]. Выпадение неспецифических реакций в ИФА может быть обусловлено техническими причинами и развиваться в результате взаимодействия белков сыворотки или конъюгатов с твердой фазой и белок - белковых взаимодействий, связанных с перекрестными реакциями между антителами и антигенами, либо сильными гидрофобными связями крупных комплексов с белками на носителе [29]. Одним из наиболее простых и быстрых в постановке трепонемных тестов является реакция с сенсибилизированными эритроцитами, или РПГА, впервые примененная при сифилисе G.Blumental и W.Bachman в 1932 году и детально изученная Т.Rathlev (1967) и Т.Tomizawa et al. (1966) [31, 154, 174]. Приоритет применения данной реакции в России принадлежит В.Н.Бедновой и Г.Ф.Тимченко (1987) [5]. По мнению многих авторов [18, 19, 174] РПГА является достаточно специфичной, с ее помощью можно дифференцировать положительные результаты РСК с кардиолипиновым АГ и протеином Рейтера на обусловленные сифилисом и неспецифические. Однако, как оказалось, эта реакция также способна давать ЛПР при целом ряде заболеваний: лепра, диффузные болезни соединительной ткани, инфекционный мононуклеоз, гетерофильные реакции с несенсибилизированными эритроцитами[18, 52, 121, 167]. Таким образом, ни один из применяемых в настоящее время трепонемных тестов не стал реакцией-арбитром, поскольку все они в ряде случаев могут сами оказаться ложноположительными или ложноотрицательными. Кроме того, следует отметить, что у большинства пациентов после успешного лечения сифилиса трепонемные тесты остаются положительными на очень долгое время, а иногда - в течение всей жизни [20, 25, 38, 133]. Нетрепонемные тесты, по изменению позитивности которых оценивают эффективность проведенной противосифилитической терапии, в ряде случаев, как было указано раннее, дают ложноположительные результаты и затрудняют определение дальнейшей тактики ведения пациента. Таким образом, в настоящее время современная сифилидология нуждается в принципиально новых подходах к диагностике сифилитической инфекции. Необходим такой метод, с помощью которого возможно выявлять заболевание на любой стадии и при любой форме течения инфекции, вне зависимости от состояния иммунной системы человека, биологических факторов, отягощенности соматического статуса, технических особенностей, и который мог бы служить критерием оценки эффективности проведенного специфического лечения. В последние годы одним из перспективных направлений при создании методов диагностики различных заболеваний является использование протеомных технологий, область применения которых тесно связана с поиском диагностических маркеров заболевания [50, 60]. Основной идеей такой целевой «маркерной» диагностики является идентификация определенных молекул или их комплексов, которые присутствуют только в пораженных тканях или клетках (но отсутствуют в нормальных) и/или выделяются во внешнюю среду или внутренние среды организма. Любой биологический процесс сопровождается каскадами ферментативных реакций, и специфичный набор их продуктов-фрагментов белков можно обнаружить в крови [152]. Протеомные технологии позволяют получать информацию сразу о больших совокупностях белков и сравнивать их наборы у больных и здоровых людей. В применении протеомных технологий к выявлению биомаркеров можно условно выделить два разных подхода [11]. Первый подход использует новые технические возможности для поиска биомаркеров и их дальнейшей идентификации, после чего найденные маркеры можно использовать в диагностике аналогично применяемым в настоящее время (например, иммунными методами). Другой подход основан на сравнении протеомного профиля в целом для больных и здоровых людей с привлечением статистических методов для выявления значимых различий, не предполагая обязательной идентификации биомаркера. При этом диагностическим признаком является сам состав протеомного профиля, т.е. исследования и непосредственная диагностика могут проводиться одним и тем же методом. Протеомика - направление молекулярной биологии, занимающееся сравнительным изучением клеточных протеомов, т.е. всех белков, которые могут быть экспрессированы геномом данной клетки в определенный момент времени [185]. Ее основной задачей является предсказание функциональной роли отдельных белков путем экспериментального сопоставления их качественного и количественного составов в разных клетках, а также установление взаимосвязи между структурой белка и его функциями [108]. Общее число различных белков в организме человека исчисляется миллионами, идентифицировать которые можно только путем их непосредственного анализа. Белки обладают различными свойствами: электрическим зарядом, размером, гидрофобностью, что используют для их разделения и последующей идентификации. Объектами исследования могут являться биологические жидкости (плазма или сыворотка крови, спинномозговая, синовиальная, амниотическая, бронхоальвеолярная жидкости, моча), клетки и биоптаты тканей человека, а также протеомы микроорганизмов - возбудителей заболеваний [11, 21, 62, 126]. Методическая база протеомики включает набор высокопроизводительных методов разделения и анализа, направленных на получение исчерпывающей информации о биохимических свойствах белков в живых системах (уровень экспрессии, посттрансляционные модификации, их взаимоотношения друг с другом) [14]. В настоящее время в протеомном анализе можно условно выделить несколько этапов: подготовка проб, фракционирование белков, идентификация белков. Подготовка проб. Опыт протеомных исследований показывает, что проблеме подготовки проб необходимо уделить особое внимание, поскольку существуют объективные факторы, способные резко ухудшить разделение белков и, следовательно, сделать невозможным объективную интерпретацию результатов [14]. Так, большинство биопсийных и аутопсийных проб представляют собой клетки разной тканевой принадлежности (соединительная ткань, органоспецифические клетки, клетки крови и т.д.), что делает интерпретацию результатов затруднительной. В последнее время в протеомных исследованиях стали применять технологию лазерной микродиссекции (LCM) (Laser Capture Microdissection) для выделения гомогенной по составу клеточной популяции непосредственно из тканей биопсийных материалов [14]. Подготовка проб для протеомного анализа облегчена, когда используют биологические жидкости организма (плазма и сыворотка крови, синовиальная и спинномозговая жидкости, моча) или лизаты клеток, поскольку в этих препаратах белки уже находятся в растворенном состоянии. Наиболее простой способ дезинтеграции клеток - использование стандартных лизирующих растворов. В некоторых случаях применяют процедуру «замораживание - оттаивание», а также обработку ультразвуком. Фракционирование белков. В настоящее время для разделения белков в протеомных исследованиях широко используются два основных подхода: двумерный (2D)-электрофорез и многомерную хроматографию. Метод 2D-электрофореза основан на фракционировании белков [59, 128, 136]. При осуществлении метода белки разделяют по двум различным физико-химическим свойствам: в начале идет разделение в первом направлении по заряду согласно их изоэлектрической точке путем изоэлектрического фокусирования (ИЭФ), а затем во втором направлении - согласно их молекулярной массе с помощью электрофореза. Обе процедуры проводят в полиакриламидном геле (ПААГ). В результате проведения 2D-электрофореза получают двумерную «белковую карту». За один раз методом двумерного гель-электрофореза можно разделить до 2000 отдельных полипептидных цепей. Разрешение этого метода настолько велико, что позволяет разделить два практически идентичных белка, отличающихся одной заряженной аминокислотой. После разделения белков методом 2D-электрофореза проводят их визуализацию с помощью окрашивания: коллоидным раствором кумасси [146], серебром (нитратом серебра с тиосульфатом натрия) [145], специальными флуоресцентными красителями SYPRO Ruby [195]. Для выявления биомаркеров сравнивают «протеомные карты» образцов при патологическом состоянии и в норме, обнаруживая белки, уровень экспрессии которых изменяется при развитии патологии [11]. Далее эти белки вырезают из геля и проводят гидролиз какой-либо эндопептидазой, например трипсином (трипсинолиз) для получения коротких (в среднем 10-15 аминокислотных остатков) пептидов, которые идентифицируют на следующем этапе анализа. Однако данный метод сложен в исполнении, мало поддается автоматизации и вследствие этого имеет низкую производительность [14]. Кроме того, одним из недостатков в отношении поиска биомаркеров является неудобство применения двумерного электрофореза для разделения низкомолекулярных белков и пептидов. Многомерная хроматография представляет группу хроматографических методов, использующих разнообразные сорбенты, но, как правило, одну систему элюентов для проведения хроматографического разделения фрагментов белков после их гидролиза (трипсинолиза) [14]. В большинстве случаев носитель состоит из двух сорбентов - сильного катионообменника и обращенной фазы [186, 196]. Протеомные методы, основанные на многомерной хроматографии, очень многообразны. К ним относят высокоэффективную жидкостную хроматографию (ВЭЖХ), имеющую высокую производительность, позволяющую существенно повысить разрешающую способность хроматографического разделения пептидов и поднять чувствительность масс-спектрометрического определения белков [94], двумерную (2D)-хроматографию, позволяющую существенно расширить набор используемых для солюбилизации белков при подготовке проб органических растворителей, детергентов и поверхностно-активных веществ [129], а также метод SELDI (Surface-Enhanced Laser Desorbtion lonization), основанный на применении белковых микрочипов и обладающий высокой чувствительностью и легкой адаптацией к диагностическому формату [109, 180]. Идентификация белков. Идентифицируют белки и пептиды, находящиеся в биологическом материале, с помощью методов масс-спектрометрии. Они позволяют получать спектры распределения белков в смеси по массе: каждому белку соответствует определенный пик, положение которого определяется соотношением массы и заряда белка, а интенсивность неявным образом отражает количество белка. При сопоставлении масс-спектров образцов биологического материала от больных и здоровых возможно выявлять белки и пептиды, являющиеся специфичными для данного заболевания. В процессе осуществления масс-спектрометрического анализа исследуемые белки предварительно с помощью протеолиза фрагментируют до пептидов (обычно трипсином), которые затем подвергают ионизации. В настоящее время для ионизации органических соединений, в том числе белков, используют в основном два метода: матричную лазерную десорбционную ионизацию (MALDI), в результате которой образуются в основном однозарядные ионы белков, хотя могут наблюдаться и двух-, и трехзарядные ионы, и метод ионизации в электроспрее (ESI), итогом которого является образование пула многозарядных ионов [14]. После получения ионов начинается второй этап масс-спектрометрического анализа - сортировка ионов по массам (точнее, по отношению массы к заряду, или m/z), происходящий в той части масс-спектрометра, которая называется «масс-анализатором». Существует несколько типов масс-анализаторов. В современных протеомных исследованиях широко используются времяпролетные масс-спектрометры (Time-of-Flight, ToF), которые хорошо сочетаются с MALDI. MALDI-TOF-масс-спектрометры позволяют проводить прямой масс-спектрометрический анализ белков сыворотки крови (прямое белковое профилирование) и получать уникальные масс-спектры с высокой точностью и разрешением, характеризующие исследуемый объект по типу «отпечатков пальцев» [65]. Они позволяют очень быстро анализировать большое количество образцов, требуют сравнительно небольшого количества биологического материала, обладают высокой чувствительностью и хорошим разрешением для низкомолекулярных белков и пептидов, что делает особенно перспективным их использование для поиска биомаркеров. Следующим этапом по фрагментам пептида возможно установить их аминокислотную последовательность. Существуют базы данных, содержащие аминокислотные последовательности белков, и, осуществляя запрос по базе данных по известной пептидной последовательности, идентифицируется белок [14]. Для обнаружения биомаркеров заболеваний была также разработана технология SELDI-TOF, совмещающая в себе масс-спектрометрическую детекцию белков с использованием белковых чипов. В качестве биологического материала для исследования с помощью метода SELDI-TOF могут использоваться как белковые экстракты из тканей, так и биологические жидкости (плазма или сыворотка крови, моча). Однако сыворотка крови является сложной смесью, в которой в больших концентрациях присутствуют мажорные белки (например, альбумин). И можно предположить, что в условиях конкуренции за место связывания с поверхностью чипа преимущество будут иметь мажорные белки, тогда как потенциальные биомаркеры, присутствующие в следовых количествах, просто не свяжутся с чипом. По этой же причине количество связавшегося белка, и, следовательно, интенсивность пика может зависеть не только от его количества, но и от концентрации других белков в сыворотке [82]. Поэтому реальные пределы чувствительности метода при работе не с изолированными белками, а со сложной смесью, такой как сыворотка крови, пока не определены. На данном этапе технология SELDI-TOF широко применяется для разработки диагностики различных видов рака, оставаясь при этом в значительной степени эмпирическим методом [11]. Разрешение методов масс-спектрометрии возможно улучшить путем применения тандемной масс-спектрометрии (MS/MS), при которой используются два масс-спектрометра [14]. Принцип метода состоит в том, что ионизированные пептиды, выбранные по массе в первом масс-спектрометре, подвергаются дальнейшей фрагментации при столкновении с газом во втором, и по фрагментам пептида устанавливается их аминокислотная последовательность. В настоящее время одной из перспективных систем, предназначенных для решения задач клинической протеомики, является система CLINPROTТМ производства компании «Bruker Daltonics», включающая средства для фракционирования, измерения и визуализации профилей пептидов и белков, программное обеспечение для обработки полученных данных. В основе метода фракционирования лежат различные виды хроматографии в объеме (ионообменная, металло-аффинная, хроматография гидрофобных взаимодействий). Использование робота ClinProtRobot обеспечивает автоматизацию очистки пробы, ее фракционирования и подготовки соответствующей мишени для масс-спеткрометрического анализа. Профильные спектры разделенных биомолекул регистрируются масс-спектрометром MALDI-TOF microflex, позволяющим распределять большое количество белков и пептидов по соотношению масса/заряд в биологическом образце, или MALDI-TOF ultraflex, позволяющим обработать каждый пептид и определить последовательность аминокислот, образующих целевой пептид. Последовательность аминокислот дает возможность искать в базах данных протеин, который может являться специфичным для данного заболевания, по сути, являясь его маркером. Обработка данных осуществляется с помощью программного обеспечения ClinProToolsТМ, которое позволяет сравнивать большие объемы данных, а также распознавать сложные комбинации биомаркеров. Таким образом, в масс-спектрах определяют пики, по которым выявляются наиболее достоверные различия между больными и здоровыми в отношении данного заболевания, что, по сути, является маркером заболевания. Полученные пики можно применять не только в качестве объекта исследования, но и как диагностический признак [11]. Задача исследователей заключается в подборе условий для получения наиболее информативных и воспроизводимых спектров и выработке правила, в соответствии с которым тот или иной спектр можно было бы классифицировать как «здоровье» или «болезнь». Возможности протеомных технологий сразу привлекли внимание исследователей в области медицины. Наибольшее число исследований посвящено поиску биомаркеров онкологических заболеваний [56, 57, 64, 76, 84, 90, 91, 96, 97, 102, 104, 105, 122, 127, 137, 141, 162, 163, 164, 171, 172, 184, 190, 192, 194, 197, 198]. Показано, что путем сравнения «белковых карт» двумерного электрофореза белков, выделенных из разных опухолей, можно изолировать белки, экспрессия которых закономерно повышается или понижается в клетках определенных новообразований. MALDI-TOF позволяет быстро идентифицировать и изучить все дифференциально экспрессирующиеся белки. К настоящему моменту опубликован ряд работ по разработке метода диагностики рака яичников с применением протеомных технологий. Большинство исследователей ставили задачу выявления значимых отличий в спектрах у больных и здоровых людей без выяснения природы этих отличий, и разработки на их основе правила диагностики [120, 152, 183, 202], а другие - идентифицировали различающиеся пики [142, 200]. Необходимо отметить, что наборы потенциальных биомаркеров, полученные разными исследователями, совершенно разные. Только 2 белка встречаются более чем в одной работе: это маркер массой примерно 11,7 кДа [142, 183], идентифицированный как сывороточный амилоид А1 [142], и маркер с массой примерно 28 кДа [120, 200], идентифицированный как аполипопротеин А1 [200]. Сывороточный амилоид А1 - известный белок воспаления, уровень которого повышается при многих инфекционных заболеваниях, травмах и воспалительных процессах [181]. Есть данные о повышении его концентрации в крови при раке легких [106, 117] и почек [118]. Аполипопротеин А1 продуцируется печенью и его концентрация напрямую связана с наличием или отсутствием воспалительного процесса [74]. Идентифицированные белки являются продуктами не самой раковой ткани, а печени и, следовательно, повышение их концентрации в крови является следствием системного ответа организма на присутствие злокачественного образования. По-видимому, изменение концентрации найденных биомаркеров может быть вызвано не только раком, но и другими воспалительными процессами [11]. Petricoin и соавторы [152] на основании результатов сравнения протеомного профиля плазмы больных, страдающих раком яичников и различными доброкачественными образованиями, правильно определили больных I стадией рака яичников и тех, кто имеет II-IV стадии. Из 66 больных доброкачественными новообразованиями яичника у 3 был неправильно диагностирован рак яичников. Можно предположить, что воспалительные заболевания и доброкачественные опухоли имеют собственные характерные профили экспрессии белков. Важно отметить, что практически во всех случаях в качестве биомаркеров выявлены не один или два, а целый ряд белков, разнообразных по структуре и функциональным свойствам. Использование нескольких маркеров способствует увеличению чувствительности и специфичности метода диагностики [11]. С помощью протеомных технологий ведется поиск биомаркеров при заболевании раком носоглотки [78]. При сравнении протеомных профилей сыворотки крови пациентов с раком носоглотки и здоровых людей обнаружены два белка с молекулярными массами 11,6 и 11,8 кДа, представляющие собой две изоформы сывороточного амилоида A (SAA), содержание которых значительно повышено у больных со злокачественной опухолью носоглотки. Длительный мониторинг больных показал, что уровень SAA в сыворотке крови значительно повышается при рецидиве болезни. При исследовании методом 2D-электрофореза в сочетании с масс-спектрометрией биоптатов эпителиальной ткани рака легкого обнаружены белки, имеющие диагностическую значимость. Выявленные белки включают: 15-гидрокси простагландин-дегидрогеназу, 3-гидроксиметилглутарилкоэнзим А-синтетазу, аполипопротеин J, бета-глюкоронидазу, флавинредуктазу, CuZn-суперокисиддесмутазу, катепсин Д, белок теплового шока 27 и др. [135]. При протеомном профилировании мочи пациентов с карциномой почки обнаружен ряд ферментов, контролирующих метаболизм, уровень экспрессии которых значительно повышен по сравнению с нормой [151]. Обнаруженные белки принимают участие в таких важнейших метаболических процессах, как гликолиз, метаболизм пирувата, цикл превращения мочевины. При исследовании белкового профиля биологических образцов пациентов с раком простаты найдены белки аннексии I, II и VII, уровень экспрессии которых различается для больных и здоровых людей [168]. Основные протеомные исследования в дерматологии сосредоточены на поиске биомаркеров опухолевого роста при таких заболеваниях, как плоскоклеточный рак [148, 201] и меланома [139, 189]. В этих исследованиях протеомный профиль изучается как в образцах ткани опухоли, так и в биологических жидкостях пациентов: крови и слюне [86]. Методом 2D-электрофореза в сочетании с масс-спектрометрией в слюне больных плоскоклеточным раком обнаружены 2 белка: Протеомные исследования широко применяются в изучении псориаза [73]. В ходе анализа белкового профиля псориатической кожи методом 2D-электрофореза с последующим микросиквенированием белков кератиноцитов выявлено 6 белков, экспрессия которых при псориазе повышена в 5 и более раз по сравнению с нормой, с кажущимися молекулярными массами 40,3 кДа, 12,4 кДа, 11,9 кДа, 11,6 кДа, 11,6 кДа и 10,1 кДа. При сравнении протеомного профиля разных форм псориаза (бляшечной и каплевидной) и здоровой ткани установлено, что независимо от формы заболевания увеличивается экспрессия белков SCCA-2 и RhpoGDI и белков HSP27 и 14-3-3 Кроме того, проводятся исследования протеомного профиля при различных аутоиммунных заболеваниях [107], таких как красная волчанка [176], склеродермия [92], витилиго [131]. При исследованиях применялись 2D-электрофорез и масс-спектрометрия, SELDI; в качестве субстрата использовались сыворотка крови, синовиальная жидкость, биоптаты тканей. Полученные данные свидетельствуют, что в патогенезе аутоиммунных заболеваний особую роль играют цитокины, хемокины, а также белки, связанные с процессами апоптоза. Возможность использования протеомных технологий для диагностики заболеваний активно изучается в ревматологической практике. Проведены исследования различий белкового профиля сыворотки крови у больных остеоартритом и ревматоидным артритом [193]. В сыворотке крови у больных ревматоидным артритом идентифицировано почти 90 белковых субъединиц, которые отсутствовали у пациентов с остеоартритом. При протеомном анализе белков плазмы крови и синовиальной жидкости у пациентов с различными формами артрита выявлены: 1) продукты деградации Имеются отдельные исследования по применению протеомного профилирования плазмы крови больных с патологией сердечно-сосудистой системы и нарушения мозгового кровообращения [188]. Показано, что, по меньшей мере, 177 белков плазмы крови можно использовать как диагностические маркеры. Имеются единичные исследования по применению протеомного профилирования плазмы крови больных инфекционными заболеваниями. В результате протеомного анализа плазмы крови больных атипичной пневмонией (SARS) были идентифицированы 38 белков, большинство из которых характерны для острой фазы заболевания и появляются в крови больных SARS вследствие целого ряда процессов, вызванных действием SARS-коронавируса [75]. Среди них гаптоглобин, который широко используется в качестве маркера воспаления при диагностике инфекционных и воспалительных поражений в ветеринарной медицине [87], маннозасвязывающий белок, относящийся к семейству пектинов С-типа и тесно связанный с инфекционными заболеваниями [88], иммунным ответом при инфицировании вирусом гриппа А типа [100] и ВИЧ [179]. В научной литературе нет данных о результатах использования протеомного профилирования сыворотки крови для изучения сифилитической инфекции. Однако с учетом имеющихся сведений о методологии протеомных технологий, возможности использования в качестве материала для исследования сыворотки крови, при получении которой не требуется специального оборудования и не создаются неудобства для пациента, метод протеомного профилирования можно считать перспективным для разработки новой технологии специфической диагностики сифилиса. Использование знаний о протеомном составе сыворотки или плазмы крови в совокупности с высокопроизводительным аналитическим инструментом протеомики - масс-спектрометрическим анализом белков - предоставляет возможность принципиально нового подхода к диагностике сифилитической инфекции, способного преодолеть ограничения классических методов. Раскрытие настоящего изобретения Сущностью настоящего изобретения является способ, с помощью которого возможно выявлять сифилис на любой стадии и при любой форме течения, вне зависимости от состояния иммунной системы человека, биологических факторов, отягощенности соматического статуса, технических особенностей и который может служить критерием оценки эффективности проведенного специфического лечения. Таким образом, настоящее изобретение относится к способу диагностики сифилиса у пациента методом прямого протеомного профилирования сыворотки крови на основе выявления в опытном образце сыворотки биомаркеров сифилиса, предусматривающему следующие стадии: а) фракционирование белков сыворотки с использованием магнитных частиц; б) масс-спектрометрический анализ образца элюата, полученного на стадии а); в) анализ полученного масс-спектра на предмет наличия или отсутствия набора пиков, соответствующих биомаркерам сифилиса, причем наличие характерного набора пиков в масс-спектре свидетельствует о наличии сифилиса, а отсутствие характерного набора пиков в масс-спектре свидетельствует об отсутствии сифилиса у пациента. В соответствии с одним из вариантов выполнения настоящего изобретения магнитные частицы представляют собой MB-WAX (магнитные микрочастицы с положительно заряженными функциональными группами на поверхности). В соответствии с одним из предпочтительных вариантов выполнения настоящего изобретения масс-спектрометрический анализ образца элюата осуществляют по методу MALDI-TOF. Следует, однако, понимать, что для осуществления настоящего изобретения могут быть применены и другие типы микрочастиц, а также альтернативные методы масс-спектрометрии. В соответствии с одним из вариантов выполнения настоящего изобретения сифилис представляет собой ранний скрытый сифилис, характерный набор биомаркеров которого характеризуется значениями соотношения молекулярной массы к заряду (m/z) 2453,67; 4296,44; 2729,63; 10672,86; 2623,83; 7199,98; 6078,82; 7934,44; 2011,07; 2644,48. В соответствии с другим вариантом выполнения настоящего изобретения сифилис характеризуется манифестным течением и представляет собой первичный или вторичный сифилис, характерный набор биомаркеров которого характеризуется значениями соотношения молекулярной массы к заряду (m/z) 2452,18; 2600,42; 2642,96; 2727,81. Вариант осуществления настоящего изобретения Условия проведения исследования, определяющие значимость его результатов Для проведения исследований по поиску биомаркеров, специфичных для сифилитической инфекции, использовали 60 образцов сывороток крови, полученных от 60 больных ранними формами сифилитической инфекции, среди которых 30 пациентов с манифестным (первичным и вторичным) и 30 - с ранним скрытым сифилисом. Диагноз был подтвержден положительными результатами стандартных серологических реакций (РПР, РПГА, ИФА), регламентированных в Российской Федерации для диагностики заболевания, обнаружением возбудителя сифилитической инфекции (Treponema pallidum) в отделяемом эрозивных/язвенных специфических элементов, клиническими данными. Контроль составили 30 образцов сывороток крови, полученных от здоровых лиц. Основным критерием включения в группу контроля являлся отрицательный результат стандартных серологических реакций (РПР, РПГА, ИФА), регламентированных в Российской Федерации для диагностики сифилиса. Исследуемые группы были сопоставимы по полу и возрасту. В исследование не включали образцы сывороток крови, полученные от пациентов с тяжелыми сопутствующими заболеваниями внутренних органов, с указанием на лекарственную зависимость или постоянное употребление алкоголя, беременных. Методология исследования: 1) пробоподготовка (фракционирование белков сыворотки крови) 2) масс-спектрометрия 3) анализ полученных данных 1. Фракционирование белков сыворотки крови Для фракционирования использовались магнитные микрочастицы MB-WAX (магнитные микрочастицы с положительно заряженными функциональными группами на поверхности, что позволяет проводить анионообменную хроматографию белков). Основой метода с использованием магнитных частиц MB-WAX является слабая анионообменная хроматография, используемая для фракционирования белков по заряду ионов. Процедура проводится в соответствии с протоколом производителя: Подготовка магнитных частиц для фракционирования 1. Смесь магнитных частиц (МВ-WAX) тщательно перемешивали в течение 1 минуты до состояния гомогенной суспензии на вортексе. 2. К 10 мкл магнитных частиц, тщательно пипетируя, добавляли 20 мкл буфера для активации (АВ). 3. Пробирку помещали со смесью магнитных частиц и буфера в магнитный сепаратор на 20 секунд для активации. 4. Супернатант аккуратно удаляли пипеткой, не касаясь образовавшегося осадка магнитных частиц. 5. Для уравновешивания магнитных частиц добавляли 100 мкл связывающего буфера (ВВ). 6. Пробирку помещали со смесью магнитных частиц и буфера в магнитный сепаратор на 20 секунд для связывания. 7. Супернатант аккуратно удаляли пипеткой, не касаясь образовавшегося осадка магнитных частиц. 8. Шаги 5-7 повторяли. 9. Осадок магнитных частиц ресуспендировали в 20 мкл связывающего буфера (ВВ). Процедура фракционирования белков 1. В раствор ресуспендированных магнитных частиц вносили 5 мкл пробы и 5 раз пипетировали для смешивания магнитных частиц с пробой. 2. Магнитные частицы инкубировали с пробой в течение 5 минут при комнатной температуре. 3. После инкубации пробирки помещали в магнитный сепаратор на 20 секунд для отделения не связавшихся белков от магнитных частиц. 4. Через 20 секунд пробирки снимали с магнитного сепаратора и супернатант аккуратно удаляли пипеткой, не касаясь образовавшегося комплекса в виде осадка. 5. К осадку магнитных частиц добавляли 100 мкл связывающего буфера (ВВ), тщательно пипетируя смесь. 6. Пробирку с магнитными частицами и промывочным буфером (ВВ) инкубировать в течение 20 секунд для образования осадка магнитных частиц на стенке пробирки в магнитном сепараторе. 7. Через 20 секунд пробирку снимали с магнитного сепаратора и супернатант аккуратно удаляли пипеткой, не касаясь образовавшегося осадка магнитных частиц. 8. Шаги 5-7 повторяли два раза. 9. Для элюирования связавшихся белков к осадку магнитных частиц добавляли 10 мкл элюирующего буфера (ЕВ) и тщательно перемешивали. 10. Инкубировали при комнатной температуре в течение 5 минут. 11. После инкубации пробирку помещали в магнитный сепаратор для отделения элюата от магнитных частиц на 30 секунд. 12. Пробирку снимали с магнитного сепаратора, аккуратно отделяли элюат от магнитных частиц и переносили в другую пробирку. Выделенная фракция белков предназначалась для масс-спектрометрического анализа (MALDI-TOF). 2. Масс-спектрометрия Масс-спектрометрический анализ проводили с использованием MALDI-TOF (времяпролетного) масс-спектрометра Bruker Microflex (Bruker Daltonics, Германия), оснащенного азотным лазером ( Для управления масс-спектрометром, включая установку режимов работы и регистрации масс-спектров, использовали программный пакет flexControl 2,4 (Bruker Daltonics, Германия). 3. Анализ полученных данных Разметку масс-спектров, выделение сигналов, статистический анализ экспериментальных данных, полученных в виде масс-спектров, и построение моделей классификаторов проводили с использованием программного пакета для обработки данных клинических масс-спектрометрических анализов ClinProTools версия 2,1 (Bruker Daltonics, Германия), отвечающего всем главным требованиям поиска биомаркеров в сложных биологических смесях и их валидации. В биоинформатической системе ClinProTools (версия 2,1) реализованы два метода построения классификационных моделей (классификаторов) для анализа распределения биомаркеров между группами: метод опорных векторов (Support Vector Machine -SVM) и генетический алгоритм (GA), являющиеся общепризнанными и эффективными методами математического анализа масс-спектрометрических данных для решения задач, связанных с построением классификаторов. Определение биомаркеров, выявляемых в моделях с помощью данных алгоритмов как масс-спектрометрические сигналы, осуществляется путем подбора оптимальных параметров алгоритмов: количество заданных масс-спектрометрических сигналов (пиков) и количество «соседей» (для обоих алгоритмов), количество итераций (для генетического алгоритма) до достижения наивысших показателей кросс-валидации (Cross-Validation) и способности к распознаванию (Recognition Capability). В результате масс-спектрометрического анализа белков/пептидов сыворотки крови больных ранним скрытым сифилисом с использованием классификатора SVM определены 20 значимых масс-спектрометрических сигналов (пиков), с использованием классификатора GA - 10. Обнаружено, что в обеих моделях, построенных с использованием вышеуказанных классификаторов, совпадают 10 пиков со средним значением отношения молекулярной массы к заряду (m/z): 2453,67; 4296,44; 2729,63; 10672,86; 2623,83; 7199,98; 6078,82; 7934,44; 2011,07; 2644,48. Пики, полученные в обеих моделях, приведены в таблицах 1 и 2. Следует отметить, что все десять пиков, полученных с использованием классификатора GA, входят в число двадцати пиков, полученных с использованием классификатора SVM, а, следовательно, соответствуют наиболее достоверным маркерам раннего скрытого сифилиса, характерному набору биомаркеров раннего скрытого сифилиса.
В результате масс-спектрометрического анализа белков/пептидов сыворотки крови больных с манифестным (первичным и вторичным) течением сифилиса с использованием обоих классификаторов (SVM и GA) определены 10 значимых масс-спектрометрических сигналов (пиков). Обнаружено, что в обеих моделях, построенных с использованием вышеуказанных классификаторов, совпадают 4 пика со средним значением отношения молекулярной массы к заряду (m/z): 2452,18; 2600,42; 2642,96; 2727,81, которые соответствуют наиболее достоверным маркерам манифестного сифилиса, характерному набору биомаркеров манифестного сифилиса. Пики, полученные в обеих моделях на сыворотке крови больных с манифестным течением сифилиса, приведены в таблицах 3 и 4.
1. Способ диагностики сифилиса у пациента методом прямого протеомного профилирования сыворотки крови на основе выявления в опытном образце сыворотки биомаркеров сифилиса, предусматривающий следующие стадии: 2. Способ по п.1, в соответствии с которым магнитные частицы представляют собой MB-WAX. 3. Способ по п.1, в соответствии с которым масс-спектрометрический анализ образца элюата осуществляют по методу MALDI-TOF. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



 87 от 26.03.2001 г. «О совершенствовании серологической диагностики сифилиса», с 2006 года на территории Российской Федерации призваны заменить КСР [38].
87 от 26.03.2001 г. «О совершенствовании серологической диагностики сифилиса», с 2006 года на территории Российской Федерации призваны заменить КСР [38]. -1-В-гликопротеин и фактор В комплемента, отсутствующие в слюне здоровых людей [148]. У больных меланомой выявляется несколько видов белков с молекулярной массой около 30 кДа, которые отсутствуют в сыворотке крови здоровых людей. Количество пептидов с молекулярными массами 2,5-3,5 кДа у больных меланомой зависит от клинической стадии заболевания [86].
-1-В-гликопротеин и фактор В комплемента, отсутствующие в слюне здоровых людей [148]. У больных меланомой выявляется несколько видов белков с молекулярной массой около 30 кДа, которые отсутствуют в сыворотке крови здоровых людей. Количество пептидов с молекулярными массами 2,5-3,5 кДа у больных меланомой зависит от клинической стадии заболевания [86].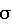 при бляшечной форме по сравнению со здоровой кожей [69].
при бляшечной форме по сравнению со здоровой кожей [69]. -цепи фибриногена в синовиальной жидкости у всех пациентов; 2) белки кальгранулина В (MRP14) и кальгранулина С исключительно в синовиальной жидкости пациентов с ревматоидным артритом; 3) фракции амилоидного А-протеина в плазме крови и синовиальной жидкости больных с ревматоидным артритом [166]. В ближайшие годы предполагают выявление многих новых биомаркерных молекул пептидов, связанных с болезнь-ассоциированными состояниями в ревматологии [153].
-цепи фибриногена в синовиальной жидкости у всех пациентов; 2) белки кальгранулина В (MRP14) и кальгранулина С исключительно в синовиальной жидкости пациентов с ревматоидным артритом; 3) фракции амилоидного А-протеина в плазме крови и синовиальной жидкости больных с ревматоидным артритом [166]. В ближайшие годы предполагают выявление многих новых биомаркерных молекул пептидов, связанных с болезнь-ассоциированными состояниями в ревматологии [153]. =337 нм), системой задержки экстракции ионов и микроканальным детектором. При работе использовали частоту импульсов лазера 20 Гц. Все измерения проводили в линейном режиме, детектируя положительно заряженные ионы с использованием ускоряющего напряжения - 20,0 кВ. Параметры масс-спектрометра оптимизировали для диапазона отношения м/z от 2000 до 20000, использовали напряжение на накапливающем электроде - 18,6 кВ и время задержки экстракции - 150 нс. Для получения каждого масс-спектра образец наносили на мишень масс-спектрометра. Мишень устанавливали в ионный источник прибора и регистрировали масс-спектры при 3000 импульсов лазера с мощностью излучения, установленной на уровне минимального значения, достаточного для десорбции-ионизации образца. Снятие спектров проводили в ручном режиме (AutoExecuteТМ, Bruker Daltonics, Германия).
=337 нм), системой задержки экстракции ионов и микроканальным детектором. При работе использовали частоту импульсов лазера 20 Гц. Все измерения проводили в линейном режиме, детектируя положительно заряженные ионы с использованием ускоряющего напряжения - 20,0 кВ. Параметры масс-спектрометра оптимизировали для диапазона отношения м/z от 2000 до 20000, использовали напряжение на накапливающем электроде - 18,6 кВ и время задержки экстракции - 150 нс. Для получения каждого масс-спектра образец наносили на мишень масс-спектрометра. Мишень устанавливали в ионный источник прибора и регистрировали масс-спектры при 3000 импульсов лазера с мощностью излучения, установленной на уровне минимального значения, достаточного для десорбции-ионизации образца. Снятие спектров проводили в ручном режиме (AutoExecuteТМ, Bruker Daltonics, Германия).














